IF 40.8|中国医学科学院发表新冠病毒最新研究成果

快速导读

严重急性呼吸系统综合征冠状病毒2(SARS-CoV-2)的变异株不断出现并逃避免疫,导致接种疫苗人群出现突破性感染。因此,迫切需要研制具有广泛保护作用的疫苗。
2024年11月6日,中国医学科学院北京协和医学院鲁帅尧教授、王佑春教授、孙强明研究员共同通讯在Signal Transduction and Targeted Therapy(IF 40.8)上发表了题为“A protein vaccine of RBD integrated with immune evasion mutation shows broad protection against SARS-CoV-2”的研究文章,初步探索并验证了以受体结合域(RBD)为免疫原,并引入有助于免疫逃逸的热点突变以开发广谱疫苗的可行性。研究表明cRBD对SARS-CoV-2变异株具有广泛的保护作用。与BA.1 RBD蛋白相比,cRBD蛋白诱导产生更高水平的广谱中和抗体,表明cRBD具有更强、更广泛的保护功效。病毒感染小鼠模型中,cRBD在减轻肺病理损伤方面比BA.1 RBD更有效。其中,cRBD3表现出最佳的广谱和保护作用。研究为SARS-CoV-2广谱疫苗研发提供思路。
康测科技为本研究提供UMI RNA-seq和UMI BCR-seq技术服务,深入探究cRBD疫苗接种后广谱差异的分子机制。其中,UMI RNA-seq揭示先天和适应性免疫途径相关基因的表达变化以及差异基因的通路富集情况。UMI BCR-seq揭示cRBD诱导的B细胞受体库差异。
研究思路
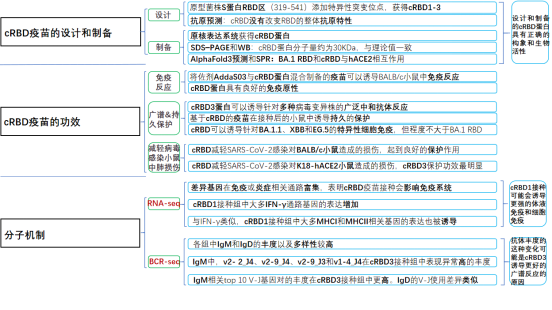
研究结果
一、cRBD疫苗的设计和制备
作者根据每个突变RBD区的免疫逃逸特性和S蛋白RBD区的抗原特性设计了新RBD序列(cRBD)(Fig. 1a)。抗原预测结果表明,cRBD没有改变RBD的整体抗原特性(Fig. 1b-d)。接着,作者使用原核表达系统获得cRBD蛋白。SDS‒PAGE和WB显示cRBD蛋白分子量约为30KDa,与理论值一致(Fig. 1e)。进一步,作者使用AlphaFold3预测BA.1 RBD和cRBD蛋白的结构以及其与人ACE2(hACE2)的结合位点(Fig. 1f-i)。表面等离子体共振(SPR)也证实了BA.1 RBD和cRBD与hACE2的相互作用(Fig. 1f-i)。这意味着设计和制备的cRBD蛋白具有正确的构象和生物活性。

二、cRBD在BALB/c小鼠中诱导强烈的免疫反应
通过采取如Fig. 2a所示的接种策略,并检测接种后6h和24h血清中细胞因子和趋化因子的表达水平(Fig. 2b)。作者发现将佐剂AddaS03与cRBD蛋白混合制备的疫苗可以诱导BALB/c小鼠中免疫反应。
考虑到目前常见的变异株大多是从BA.2进化而来,作者还检测了接种后不同天数的BA.2 RBD结合抗体水平(Fig. 2c-f)。结果表明cRBD蛋白具有良好的免疫原性。

三、cBRD3诱导产生对SARS-CoV-2变异株具有广泛中和活性的抗体
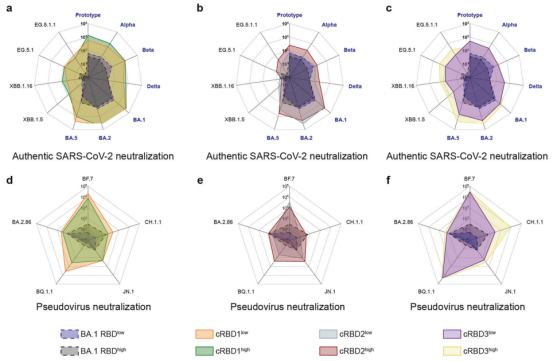
据报道,较高的nAbs水平与较低的免疫逃逸机会相关。因而,针对不同SARS-CoV-2变异株的nAbs滴度是评估疫苗保护能力广度的关键指标。作者利用SARS-CoV-2真病毒(Fig. 3a-c)和假病毒(Fig. 3d-f)中和实验检测cRBD蛋白是否可以诱导针对多种变异株的广泛中和抗体反应。作者发现cRBD3能够诱导更广泛的中和反应。此外,接种完成后18周或更长时间,小鼠血清中仍可检测到针对多种变异株的nAbs,并且cRBD接种组的抗体水平相对较高,说明基于cRBD的疫苗在接种后的小鼠中诱导持久的保护。
为了探索cRBD诱导细胞免疫的能力,作者采集了完成接种流程的小鼠的脾脏并分离淋巴细胞,同时使用BA.1.1、XBB和EG.5变异株的S蛋白作为刺激物进行ELISPOTs(Fig. 4)。结果揭示疫苗接种诱导了对BA.1.1、XBB和EG.5 S蛋白的特异性T细胞反应。然而,BA.1 RBD和cRBD接种组之间没有显著差异。综上所述,cRBD可以诱导针对BA.1.1、XBB和EG.5的特异性细胞免疫,但程度不大于BA.1 RBD。

四、cRBD减轻SARS-CoV-2感染对BALB/c小鼠造成的损伤
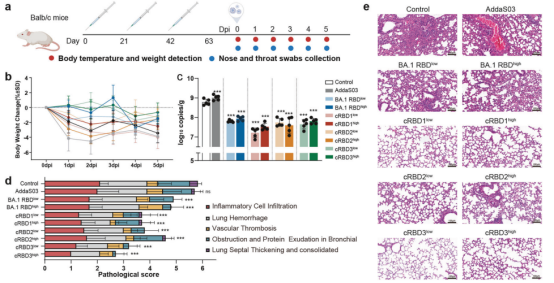
小鼠接种3次后,第63天感染SARS-CoV-2,并在感染5天后解剖。感染期每天收集鼻咽拭子、体温和体重数据(Fig. 5a)。作者发现感染EG.5.1后,各组小鼠的体重均趋于下降,cRBD3高剂量和低剂量组体重下降幅度最小(Fig. 5b)。此外,cRBD疫苗显著降低感染小鼠肺部的病毒载量(Fig. 5c)。小鼠感染病毒后肺部出现的病理变化主要表现为肺出血、炎症细胞浸润、血管血栓形成、支气管阻塞和蛋白渗出(Fig. 5d, e)。不难发现疫苗组的肺损伤程度显著低于对照组,cRBD3 疫苗的肺保护作用最强(Fig. 5d, e)。上述结果表明,cRBD减轻SARS-CoV-2感染对BALB/c小鼠造成的损伤,起到良好的保护作用。
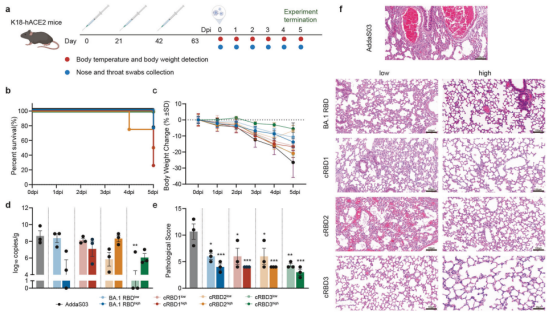
五、cRBD减轻SARS-CoV-2感染对K18-hACE2小鼠造成的损伤
为了更真实地评估cRBD疫苗的功效,作者使用K18-hACE2模型小鼠进行实验(Fig. 6a)。作者发现部分接种组小鼠在感染期出现死亡(Fig. 6b)。各组小鼠的体重在感染后均呈下降趋势。其中,佐剂组下降幅度最大,而cRBD3高剂量组下降幅度最小(Fig. 6c)。此外,基于cRBD的疫苗接种显著降低感染小鼠肺部的病毒载量。cRBD3低剂量接种组病毒载量降低尤为明显,揭示了其在抑制病毒复制方面的有效作用(Fig. 6d)。作者还发现疫苗接种显著降低感染小鼠的肺损伤,其中cRBD3接种组的肺损伤减轻最显著,这表明cRBD3可能在SARS-CoV-2感染中发挥最有效的肺保护作用(Fig. 6e, f)。总之,作者推测基于cRBD3蛋白的疫苗可能在EG.5.1感染中发挥最明显的保护作用。
六、cRBD诱导B细胞受体库差异
为了探究疫苗接种后广谱差异的分子机制,作者收集了完成3次接种后,第63天cRBD高剂量组小鼠的全血并进行RNA-seq和BCR-seq。另一组未处理的小鼠用作阴性对照(NC)组。
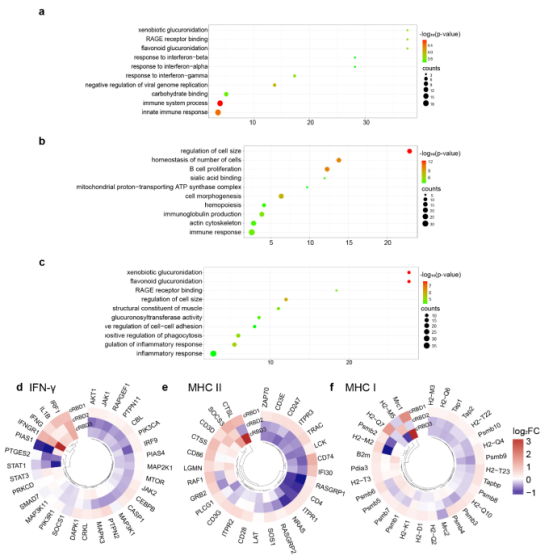
RNA-seq显示差异基因在免疫或炎症相关通路富集(Supplementary Fig. 14a-c)。这意味着cRBD疫苗接种会影响免疫系统。借助Reactome数据库,作者确定了先天和适应性免疫途径相关的基因并分析了它们的表达情况。cRBD1接种组中大多IFN-γ通路基因的表达增加,而cRBD2接种组中大多IFN-γ通路基因的表达趋于降低(Supplementary Fig. 14d)。与IFN-γ类似,cRBD1接种组中大多MHCI和MHCII相关基因的表达也被诱导(Supplementary Fig. 14e, f)。这提示cRBD1接种可能会诱导更强的体液免疫和细胞免疫。
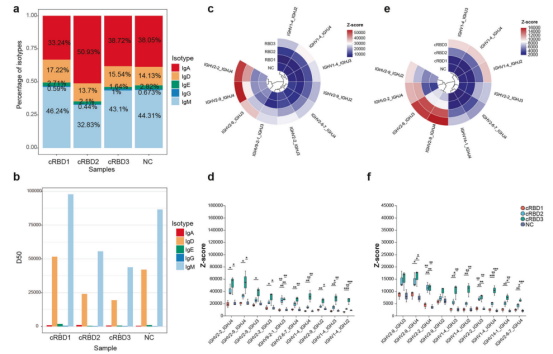
BCR-seq显示NC和cRBD疫苗接种组中IgM和IgD的丰度较高(Fig. 7a)。并且,IgM和IgD的多样性也远大于其他免疫球蛋白(Fig. 7b)。作者进一步分析了NC和cRBD疫苗接种组中IgM和IgD isoforms使用频率top 10的V-J基因对的丰度(Fig. 7c, e)。对于IgM亚型,v2- 2_J4、v2-9_J4、v2-9_J3和v1-4_J4在cRBD3接种组中表现出异常高的丰度(Fig. 7c)。统计分析表明IgM相关top 10 V-J基因对的丰度在cRBD3接种组中更高(Fig. 7d)。同样,对于IgD,V-J使用差异类似(Fig. 7f)。综上所述,作者推测抗体丰度的这种变化可能是cRBD3诱导更好的广谱反应的原因。
参考文献
Ran An, Hao Yang, Cong Tang, et al. A protein vaccine of RBD integrated with immune evasion mutation shows broad protection against SARS-CoV-2[J]. Signal Transduction and Targeted Therapy, 2024
热点推荐
点个“在看”再走呗(右下角)

更多平台
bilibili
(长干货科普)
视频号
(产品知识分享)
小红书
(短干货科普)



关于康测
康测致力于先进组学技术的开发和在生物医学研究领域的应用,建立了涵盖基因组学、表观基因组学、转录组学、表观转录组学、免疫组学和互作组学的全面组学服务体系。而在医学检测方面,康测基于自主研发的SMP(Stranded Multiplex PCR)靶向测序技术,可提供检测灵敏度和特异性均为100%的MRD一站式自动化解决方案。
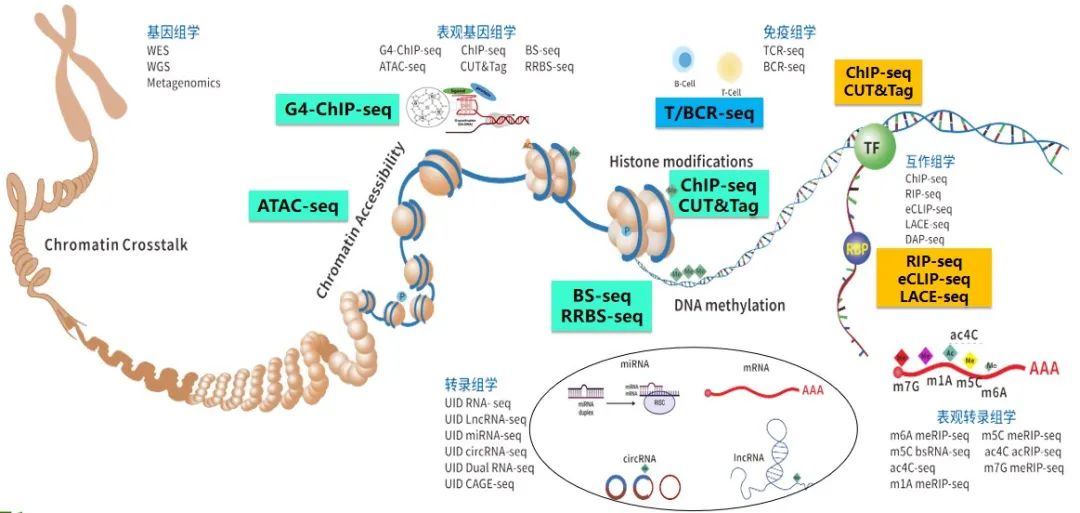
康测提供全面的基因表达调控研究工具

康测提供高度自动化MRD一站式解决方案

















